[ ความแรงของกรดเบส ]
กรด คือ สารประกอบที่มี H และเมื่อละลายน้ำจะแตกตัวให้ H+ หรือ H3O+
เบส คือ สารประกอบที่มี OH และเมื่อละลายน้ำจะแตกตัวให้ OH-
ข้อจำกัดของทฤษฎีนี้คือ สารประกอบต้องละลายได้ในน้ำ และไม่สามารถอธิบายได้ว่า ทำไมสารประกอบบางชนิดเช่น NH3 จึงเป็นเบส
[ Top ]
Bronsted-Lowry Concept
กรด คือ สารที่สามารถให้โปรตอน (proton donor) แก่สารอื่น
เบส คือ สารที่สามารถรับโปรตอน (proton acceptor) จากสารอื่น
ปฏิกิริยาระหว่างกรดกับเบสจึงเป็นการถ่ายเทโปรตอนจากกรดไปยังเบสเช่นแอมโมเนียละลายในน้ำ
NH3(aq) + H2O(1) = NH4+ (aq) + OH- (aq)
base 2 ........acid 1 ........acid 2 ........base 1
ในปฏิกิริยาไปข้างหน้า NH3 จะเป็นฝ่ายรับโปรตอนจาก H2O ดังนั้น NH3 จึงเป็นเบสและ H2O เป็นกรด แต่ในปฏิกิริยาย้อนกลับ NH4+ จะเป็นฝ่ายให้โปรตอนแก่ OH- ดังนั้น NH4+ จึงเป็นกรดและ OH- เป็นเบส อาจสรุปได้ว่าทิศทางของปฏิกิริยาจะขึ้นอยู่กับความแรงของเบส
[ Top ]

Lewis Concept
กรด คือ สารที่สามารถรับอิเลคตรอนคู่โดดเดี่ยว (electron pair acceptor) จากสารอื่น
เบส คือ สารที่สามารถให้อิเลคตรอนคู่โดดเดี่ยว (electron pair donor) แก่สารอื่น
ทฤษฎีนี้ใช้อธิบาย กรด เบส ตาม concept ของ Arrhenius และ Bronsted-Lowry ได้ และมีข้อได้เปรียบคือสามารถอธิบาย กรด เบส ในกรณีที่เกิดปฏิกิริยาระหว่างกัน และได้สารประกอบที่มีพันธะโควาเลนซ์ เช่น
OH - (aq) + CO2 (aq) HCO3- (aq)
HCO3- (aq)
BF3 + NH3  BF3-NH3
BF3-NH3
[ Top ]

ชนิดของกรดและเบส
ชนิดของกรด
1.กรด Monoprotic แตกตัว 1 ได้แก่ HNO3 , HClO3 , HClO4 , HCN
2.กรด Diprotic แตกตัว 2 ได้แก่ H2SO4 , H2CO3
3.กรด Polyprotic แตกตัว 3 ได้แก่ H3PO4
การแตกตัวของกรด Polyprotic แต่ละครั้งจะให้ H+ ไม่เท่ากัน แตกครั้งแรกจะแตกได้ดีมาก ค่า Ka สูงมากแต่แตกครั้งต่อ ๆ ไปจะมีค่า Ka ต่ำมาก เพราะประจุลบในไอออนดึงดูด H+ ไว้ดังสมการ
H2SO4 H+ + HSO4- Ka1 = 1011
HSO4- H+ + SO42- Ka2 = 1.2 x 10-2
เนื่องมาจากกรด Polyprotic มักมีค่า K1>>K2>>K3 H+ ในสารละลายส่วนใหญ่จะได้มาจากการแตกตัวครั้งแรก
ถ้าค่า K1 มากกว่า K2 =103 เท่าขึ้นไปจะพิจารณาค่า pH ของสารละลายกรด Polyprotic ได้จากค่า K1 เท่านั้น แต่ถ้าค่า K2 มีค่าไม่ต่ำมาก จะต้องนำค่า K2 มาพิจารณาด้วย
ชนิดของเบส
เบส แบ่งตาม จำนวน OH- ในเบส แบ่งได้เป็น 3 ชนิด คือ
1.เบสที่มี OH- ตัวเดียว เช่น LiOH NaOH KOH RbOH CsOH
2.เบสที่มี OH- 2 ตัว เช่น Ca(OH)2 Sr(OH)2 Ba(OH)2
3.เบสที่มี OH- 3 ตัว เช่น Al(OH)3 Fe(OH)3
[ Top ]
คู่กรดเบส
สารที่เป็นคู่กรด-เบสกัน H+ ต่างกัน 1 ตัว โดยที่ คู่กรดจะมี H+ มากกว่าคู่เบส 1 ตัว
ใน ปฏิกิริยาที่ผันกลับได้จะมีปฏิกิริยาย่อย 2 ชนิด คือ ปฏิกิริยาไปข้างหน้าและปฏิกิริยาย้อนกลับซึ่งในสารละลายกรดและสารละลายเบสจะ มีสารที่เรียกว่าคู่กรด-เบสเสมอไม่ว่าจะเป็นปฏิกิริยาใดโดยพิจารณาจากทฤษฎี กรด-เบสของเบรินสเตด-ลาวรี เช่น
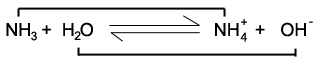
H2O เป็นคู่กรดของเบสOH-
NH3 เป็นคู่เบสของกรด NH4+
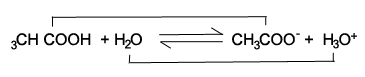
CH3COOH เป็นคู่กรดของเบสCH3COO-
H2O เป็นคู่เบสของกรด H3O+
[ Top ]

ความแรงของกรดและเบส
เบสแก่ คือ เบสที่แตกตัวได้มากหรือ เบสที่แตกตัวได้ 100 % หรือเรียกอีกชื่อหนึ่งว่า
อิเล็กโทรไลต์แก่ ได้แก่ เบสหมู่ 1 ทุกตัว และเบสหมู่ 2 ยกเว้น Be(OH)2
กรดแก่ คือ กรดที่แตกตัวได้มากหรือ เบสที่แตกตัวได้ 100 % หรือเรียกอีกชื่อหนึ่งว่า
อิเล็กโทรไลต์แก่ แบ่งออกเป็น
กรด Hydro ได้แก่ HCl , HBr , HI
กรด Oxy ได้แก่ H2SO4 , HNO3 , HClO3 , HClO4
ข้อสังเกต กรด Oxy ที่แก่ ให้นำจำนวนออกซิเจนลบกับจำนวน H+ ที่แตกตัวได้
ถ้าผลลัพธ์ตั้งแต่ 2 ขึ้นไปจะเป็นกรดแก่
[ Top ]
ไม่มีความคิดเห็น:
แสดงความคิดเห็น